Asid Hipoklorus: Kuat atau Lemah?
pengenalan
Apabila kita memikirkan asid, kita sering membayangkan sesuatu yang boleh menghakis logam atau menyebabkan kulit terbakar. Tetapi bagaimana pula dengan asid hipoklorus (HClO)? Adakah ia kuat atau lemah?
Dalam artikel yang luas ini, kami meneroka sifat HClO, faedahnya, aplikasi dan cara ia memainkan peranan penting dalam kehidupan seharian kita.
Sertai kami sambil kami menyelami kimia HClO dan temui sebab ia patut mendapat perhatian kami.
Apakah Asid Hypochlorous?
Asid hipoklorit ialah sebatian ringkas yang terbentuk apabila gas klorin larut dalam air. Ia merupakan pemain utama dalam pelbagai aplikasi, terutamanya dalam sanitasi dan pembasmian kuman.
·Komposisi Kimia: HClO terdiri daripada satu atom hidrogen, satu atom klorin, dan satu atom oksigen.
·Pembentukan: Anda mencipta HClO apabila anda mencampurkan gas klorin dengan air. Reaksi boleh diringkaskan seperti berikut:
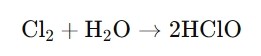
Ini menunjukkan bagaimana klorin berinteraksi dengan air untuk membentuk asid hipoklorus.
Elektrolisis: Penghasilan Asid Hipoklorus
Salah satu kaedah yang paling berkesan untuk menghasilkan asid hipoklorus (HClO) adalah melalui elektrolisis. Proses ini melibatkan penghantaran arus elektrik melalui larutan air masin, menghasilkan penjanaan HClO bersama-sama dengan produk sampingan yang lain. Mari kita mendalami cara proses ini berfungsi dan kepentingannya.
Apakah Elektrolisis?
Elektrolisis ialah proses kimia yang menggunakan tenaga elektrik untuk memacu tindak balas bukan spontan. Dalam kes pengeluaran HClO, ia melibatkan elektrolisis larutan natrium klorida (NaCl), yang biasanya dikenali sebagai garam.
Proses Elektrolisis
1.Penyediaan Penyelesaian:
· Campurkan air dengan sedikit garam (natrium klorida). Ini menghasilkan larutan garam yang akan mengalirkan elektrik.
2.Persediaan Elektrolisis:
· Larutan garam diletakkan dalam sel elektrolitik, yang mengandungi dua elektrod: anod (elektrod positif) dan katod (elektrod negatif).
3.Menggunakan Arus Elektrik:
· Apabila arus elektrik dikenakan, satu siri tindak balas elektrokimia berlaku pada elektrod.
4.Tindak balas Kimia:
· Di anod, ion klorida (Cl⁻) teroksida kepada gas klorin (Cl₂):
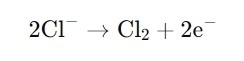
· Di katod, air dikurangkan, menghasilkan gas hidrogen (H₂) dan ion hidroksida (OH⁻):
![]()
5.Pembentukan Asid Hipoklorus:
· Gas klorin yang dihasilkan di anod bertindak balas dengan air untuk membentuk asid hipoklorus:
![]()
· Larutan yang terhasil mengandungi HClO dan spesies lain, bergantung kepada keadaan elektrolisis.
Faedah Elektrolisis untuk Pengeluaran HClO
1.Penjanaan Di Tapak:
· Elektrolisis membolehkan pengeluaran HClO di tapak, memastikan kesegaran dan mengurangkan keperluan penyimpanan.
2.Kepekatan Boleh Disesuaikan:
· Pengguna boleh melaraskan kepekatan HClO dengan mengubah suai kepekatan garam dan tempoh elektrolisis.
3.Mesra Alam:
· Proses ini menghasilkan sisa minimum, dan hasil sampingan utama (air dan garam) adalah mesra alam.
4.Kos-Efektif:
· Menghasilkan HClO melalui elektrolisis boleh menjadi lebih menjimatkan daripada membeli penyelesaian pra-dibuat, terutamanya untuk aplikasi berskala besar.
Aplikasi HClO Elektrolitik
Asid hipoklorus yang dihasilkan melalui elektrolisis mempunyai pelbagai aplikasi, menjadikannya penyelesaian serba boleh dalam industri yang berbeza.
1.Tetapan Penjagaan Kesihatan
Di hospital dan klinik, HClO elektrolitik digunakan untuk membasmi kuman permukaan dan peralatan perubatan. Keberkesanannya terhadap pelbagai jenis patogen membantu dalam kawalan jangkitan.
2.Industri Makanan
Loji pemprosesan makanan menggunakan HClO elektrolitik untuk membersihkan peralatan dan permukaan, memastikan keselamatan makanan dengan meminimumkan pencemaran mikrob.
3.Rawatan Air
Kemudahan rawatan air perbandaran menggunakan HClO yang dihasilkan daripada elektrolisis untuk membasmi kuman air minuman dan air sisa, menyediakan air yang selamat untuk komuniti.
4.Pembersihan Rumah
Banyak pembersih dan sanitizer isi rumah kini termasuk HClO elektrolitik, menyediakan cara yang selamat dan berkesan untuk membasmi kuman permukaan di rumah.
Memahami Keasidan
Untuk menentukan sama ada HClO kuat atau lemah, kita perlu memahami konsep keasidan dalam kimia.
Definisi Asid
Dalam kimia, asid ditakrifkan oleh keupayaannya untuk menderma proton (ion H⁺) kepada bahan lain.
·Teori Brønsted-Lowry: Menurut teori ini, asid ialah sebarang bahan yang boleh menderma proton.
·Teori Arrhenius: Teori ini menyatakan bahawa asid ialah bahan yang meningkatkan kepekatan ion hidrogen dalam larutan akueus.
Dengan menggunakan takrifan ini, kita boleh menilai kelakuan asid hipoklorus.
Adakah HClO Asid Kuat?
Mari kita jelaskan apa yang menjadikan asid kuat atau lemah.
·Asid Kuat: Asid kuat tercerai sepenuhnya dalam air. Ini bermakna mereka melepaskan semua ion hidrogen mereka ke dalam larutan.
·Tingkah Laku HClO: Asid hipoklorik hanya tercerai separa dalam air, membebaskan beberapa tetapi tidak semua ion hidrogen. Akibatnya,kami mengklasifikasikannya sebagai asid lemah.
Perbezaan ini adalah penting, kerana kekuatan asid mempengaruhi kereaktifan dan aplikasinya.
pH Asid Hipoklorus
Skala pH mengukur tahap keasidan atau kealkalian sesuatu larutan, antara 0 (sangat berasid) hingga 14 (sangat beralkali).
·pH biasa HClO: Asid hipoklorus biasanya mempunyai pH sekitar 5 hingga 6.5, menunjukkan keasidan sederhana.
Mengapa pH Penting?
Memahami pH HClO membantu kita mengukur cara ia berinteraksi dalam pelbagai persekitaran.
·Kesan terhadap Keberkesanan: Keberkesanan HClO sebagai pembasmi kuman meningkat dalam julat pH tertentu. Sebagai contoh, tahap pH yang lebih rendah meningkatkan sifat antimikrobnya.
·Aplikasi dalam Rawatan Air: Mengekalkan pH yang betul dalam kolam renang memastikan HClO kekal berkesan dalam membunuh mikroorganisma berbahaya.
Kebaikan Asid Hipoklorus
Apakah yang menjadikan HClO istimewa? Berikut adalah beberapa faedah utamanya:
1.Pembasmi Kuman yang Berkesan: HClO terkenal dengan keupayaannya untuk membunuh bakteria dan virus. Ini menjadikannya pilihan popular untuk sanitasi dalam pelbagai tetapan.
2.Selamat untuk Digunakan: Tidak seperti asid yang lebih kuat, HClO selamat untuk dikendalikan dan tidak merengsakan kulit. Ini amat penting dalam tetapan penjagaan kesihatan.
3.Mesra Alam: HClO terurai kepada bahan tidak berbahaya, meminimumkan kesan alam sekitar. Ia terurai menjadi garam dan air, menjadikannya pilihan yang mampan.
4.Aplikasi Serbaguna: Daripada pembersih isi rumah hinggalah kepada rawatan air, HClO didapati digunakan dalam banyak industri.
5.Tidak Toksik: Ia menimbulkan risiko minimum kepada kesihatan manusia dan selamat digunakan di kawasan penyediaan makanan.
Bagaimana HClO Berfungsi?
Mari kita terokai mekanisme di sebalik keberkesanan HClO sebagai pembasmi kuman.
Mekanisme Tindakan
·Penembusan: HClO menembusi sel mikrob, merosakkan strukturnya dan membunuhnya dengan berkesan.
·Tekanan Oksidatif: HClO menyebabkan tekanan oksidatif dalam bakteria dan virus, yang membawa kepada kematian sel.
·Keberkesanan Spektrum Luas: HClO berkesan terhadap pelbagai jenis patogen, termasuk bakteria, virus dan kulat. Kepelbagaian ini menjadikannya tidak ternilai untuk pembersihan.
Formula Ion Hipoklorit
Memahami ion hipoklorit (ClO⁻) meningkatkan pemahaman kita tentang HClO.
·Pangkalan Konjugat: Ion hipoklorit (ClO⁻) ialah asas konjugat HClO. Apabila HClO menderma proton, ia menjadi ClO⁻.
·Peranan dalam Kimia: Ion ini juga mempamerkan sifat pembasmi kuman, terutamanya dalam rawatan air. Ia sering digunakan dalam bentuk natrium hipoklorit (NaClO) dalam peluntur isi rumah.
Kestabilan Ion Hipoklorit
·Faktor Kestabilan: Kestabilan ClO⁻ boleh dipengaruhi oleh pH dan suhu. Pada tahap pH yang lebih rendah, ClO⁻ lebih stabil, menyumbang kepada keberkesanan HClO sebagai pembasmi kuman.
Aplikasi Praktikal Asid Hipoklorus
HClO menemui jalannya ke dalam banyak produk dan aplikasi. Berikut adalah beberapa kegunaan biasa:
1.Pencuci Rumah: Banyak sanitizer dan pembasmi kuman mengandungi HClO kerana sifat antibakteria yang kuat.
2.Rawatan Air: Ia adalah asas dalam memastikan kolam renang bersih dan selamat untuk berenang. HClO berkesan membunuh patogen berbahaya yang tumbuh subur dalam air kolam.
3.Penjagaan kesihatan: Digunakan dalam penjagaan luka dan tetapan pembedahan, HClO membantu mencegah jangkitan kerana sifat antibakterianya.
4.Industri Makanan: HClO sering digunakan untuk membersihkan permukaan dan peralatan yang bersentuhan dengan makanan, memastikan keselamatan makanan.
5.pertanian: Petani menggunakan HClO untuk membersihkan peralatan dan mengawal patogen dalam air pengairan.
6.Penjagaan Veterinar: Ia digunakan dalam penjagaan kesihatan haiwan untuk membasmi kuman luka dan instrumen pembedahan.
Cara Menghasilkan Asid Hipoklorus
Kami sering bergantung padaPenjana HOCluntuk pengeluaran HClO yang cekap. Begini cara ia berfungsi:
1.Campurkan Air dan Garam: Mulakan dengan menggabungkan air dan garam. Campuran ini penting untuk proses elektrolisis.
2.Gunakan Elektrolisis: Penjana menggunakan arus elektrik untuk menghasilkan HClO. Proses ini memudahkan tindak balas antara ion klorin dan air.
3.Simpan Penyelesaian: Anda boleh menyimpan penyelesaian yang dihasilkan untuk kegunaan masa hadapan. Pastikan keadaan penyimpanan yang betul untuk mengekalkan keberkesanannya.
Faedah Menggunakan Penjana HOCl
·Pengeluaran Di Tapak: Menjana HClO di tapak memastikan kesegaran dan potensi, mengurangkan keperluan untuk pengangkutan dan penyimpanan.
·Kos-Efektif: Menghasilkan HClO dengan penjana boleh menjadi lebih menjimatkan daripada membeli penyelesaian pra-dibuat.
·Kepekatan Tersuai: Pengguna boleh melaraskan kepekatan HClO berdasarkan keperluan khusus, menjadikannya serba boleh untuk pelbagai aplikasi.
Membandingkan Asid Hipoklorus dengan Asid Lain
Bagaimanakah HClO bertindan terhadap asid lain?
Berbanding Asid Kuat
·Keselamatan: Tidak seperti asid kuat seperti asid hidroklorik (HCl), HClO kurang risiko kepada kesihatan dan keselamatan manusia.
·serba boleh: HClO sesuai untuk digunakan dalam persekitaran yang sensitif, seperti penyediaan makanan dan penjagaan kesihatan.
Berbanding Asid Lemah Lain
·Keberkesanan: HClO mengatasi beberapa asid lemah dalam keberkesanan antimikrob. Sebagai contoh, asid asetik (cuka) lebih lemah dalam kuasa pembasmian kuman berbanding HClO.
Kepentingan Penggunaan yang Betul
Menggunakan HClO dengan betul memaksimumkan faedahnya. Berikut adalah beberapa petua:
1.Ikut Garis Panduan: Sentiasa patuhi kepekatan yang disyorkan untuk keselamatan. Penggunaan berlebihan atau salah guna boleh menyebabkan pembasmian kuman yang tidak berkesan.
2.Pantau Tahap pH: Mengekalkan pH dalam julat optimum memastikan HClO kekal berkesan. Ujian tetap boleh membantu mengekalkan tahap pH yang diingini.
3.Simpan dengan Betul: Simpan HClO di tempat yang gelap dan sejuk untuk mengekalkan kestabilan. Pendedahan kepada cahaya dan haba boleh merendahkan potensinya.
Membongkar Mitos Mengenai Asid Hypochlorous
Terdapat banyak salah tanggapan tentang HClO. Mari kita bincangkan beberapa:
·Mitos 1: HClO berbahaya.
·Fakta: HClO lebih selamat daripada kebanyakan asid kuat dan mempunyai potensi kerengsaan yang rendah.
·Mitos 2: Semua pembasmi kuman adalah sama.
·Fakta: HClO adalah unik kerana keberkesanan dan profil keselamatannya.
·Mitos 3: HClO mempunyai bau yang kuat.
·Fakta: Asid hipoklorit mempunyai bau yang ringan berbanding gas klorin, menjadikannya lebih menyenangkan untuk digunakan.
Contoh Dunia Nyata Penggunaan HClO
Dalam Penjagaan Kesihatan
Hospital dan klinik menggunakan HClO untuk membasmi kuman permukaan dan instrumen. Ia membantu mencegah jangkitan berkaitan penjagaan kesihatan, melindungi pesakit dan kakitangan.
Dalam Pemprosesan Makanan
Pengeluar makanan menggunakan HClO untuk membersihkan peralatan dan permukaan. Amalan ini membantu memastikan keselamatan makanan dan memanjangkan jangka hayat dengan mengurangkan pencemaran mikrob.
Dalam Kemudahan Rawatan Air
Loji rawatan air perbandaran sering menggunakan HClO untuk pembasmian kuman.
Rujukan
1.Pusat Kawalan dan Pencegahan Penyakit (CDC)- Menyahjangkit dengan Hypochlorous Acid.Panduan Asid Hipoklorus CDC
2.Jurnal Sains dan Kesihatan Alam Sekitar- Peranan HClO dalam Rawatan Air. Jurnal Sains Alam Sekitar
3.Teks Percuma Kimia- Kekuatan Asid dan Pemisahan. Kimia LibreTexts
4.Agensi Perlindungan Alam Sekitar (EPA)- Panduan Pengklorinan dan Asid Hipoklorus.Garis Panduan EPA
5.Pertubuhan Kesihatan Sedunia (WHO)- Air, Sanitasi dan Kebersihan: Garis Panduan Pembasmian Kuman.Garis Panduan Pembasmian Kuman WHO
6.Jurnal Antarabangsa Penyelidikan Alam Sekitar dan Kesihatan Awam- Keselamatan dan Keberkesanan Asid Hipoklorus. IJERPH
7.Jurnal Kawalan Jangkitan Amerika- Sifat Antimikrob Asid Hipoklorit.AJIC
8.Jurnal Perlindungan Makanan- Penggunaan Asid Hipoklorus dalam Keselamatan Makanan. Jurnal Perlindungan Makanan
9.Jurnal Jangkitan Hospital- Asid Hipoklorus sebagai Pembasmi Kuman dalam Penjagaan Kesihatan.Jurnal Jangkitan Hospital
10.Toksikologi Makanan dan Kimia- Toksikologi Asid Hipoklorus dan Penggunaannya. Toksikologi Makanan dan Kimia
